日本福岡——九州大學(xué)的研究人員揭示了DNA特定區(qū)域之間的空間距離是如何與基因活動(dòng)的爆發(fā)聯(lián)系在一起的。利用先進(jìn)的細(xì)胞成像技術(shù)和計(jì)算機(jī)建模,研究人員表明,DNA的折疊和運(yùn)動(dòng),以及某些蛋白質(zhì)的積累,取決于基因是活躍還是不活躍。這項(xiàng)研究發(fā)表在12月6日的《科學(xué)進(jìn)展》雜志上
《Nature》控制細(xì)胞行動(dòng)的新技術(shù)
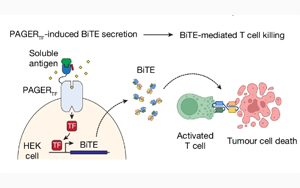
在12月4日發(fā)表在《Nature》雜志上的一篇論文中,斯坦福大學(xué)的研究人員已經(jīng)開(kāi)發(fā)出一種新的合成受體,可以容納更廣泛的輸入,并產(chǎn)生更多樣化的輸出。這項(xiàng)創(chuàng)新被稱為“可編程抗原門(mén)控G蛋白偶聯(lián)工程受體”(PAGER),圍繞G蛋白偶聯(lián)受體構(gòu)建。
Nature Cancer:腫瘤細(xì)胞分泌的EV-DNA作為一種“危險(xiǎn)”信號(hào),促進(jìn)抗轉(zhuǎn)移性免疫反應(yīng)
在12月3日發(fā)表在《自然癌癥》雜志上的這項(xiàng)研究中,研究人員檢查了癌細(xì)胞分泌的被稱為細(xì)胞外囊泡(EVs)的小膠囊包裝的短鏈DNA。所有細(xì)胞都利用EV分泌蛋白質(zhì)、DNA和其他分子,腫瘤細(xì)胞是特別活躍的EV分泌者。這些ev包裝分子的生物學(xué)功能仍在探索中,但在這種情況下,研究人員發(fā)現(xiàn),在各種癌癥類型中,腫瘤細(xì)胞分泌的EV-DNA作為一種“危險(xiǎn)”信號(hào),激活肝臟中的抗腫瘤反應(yīng),降低肝臟轉(zhuǎn)移的風(fēng)險(xiǎn)。
Nature提出了第一個(gè)直接證據(jù):支持幾十年前的多巴胺-血清素對(duì)立假說(shuō)
斯坦福大學(xué)吳蔡神經(jīng)科學(xué)研究所的一項(xiàng)新研究揭示了這些情緒管理分子的另一個(gè)新方面。這項(xiàng)研究在線發(fā)表在《自然》雜志上,首次準(zhǔn)確地展示了多巴胺和血清素是如何共同作用的——或者更準(zhǔn)確地說(shuō),是如何對(duì)立作用,來(lái)塑造我們的行為。
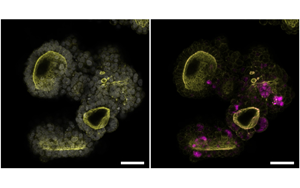
Cell:突破類器官研究限制!利用所有關(guān)鍵的胰腺細(xì)胞創(chuàng)造了一個(gè)新的類器官
來(lái)自Hubrecht研究所的類器官小組(以前的Clevers小組)的研究人員已經(jīng)開(kāi)發(fā)出一種模仿人類胎兒胰腺的新類器官,為其早期發(fā)育提供了更清晰的視角。研究人員能夠重建一個(gè)完整的結(jié)構(gòu),包括胰腺中的三種關(guān)鍵細(xì)胞類型,這是以前的類器官無(wú)法完全模仿的。
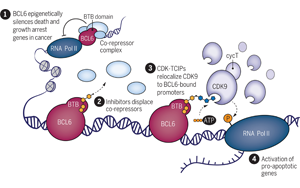
Science:突破傳統(tǒng),利用細(xì)胞自然死亡機(jī)制殺死癌細(xì)胞
斯坦福大學(xué)醫(yī)學(xué)研究人員開(kāi)發(fā)的一種新方法可能會(huì)對(duì)癌癥治療產(chǎn)生深遠(yuǎn)的影響。他們的目標(biāo)是利用這種細(xì)胞死亡的自然方法來(lái)誘騙癌細(xì)胞進(jìn)行自我處理。他們的方法是通過(guò)人為地將兩種蛋白質(zhì)結(jié)合在一起,以一種新的化合物打開(kāi)一組細(xì)胞死亡基因,最終驅(qū)動(dòng)腫瘤細(xì)胞開(kāi)啟自己的功能。
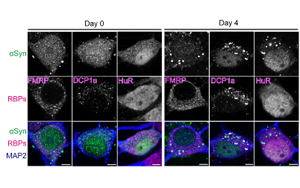
科學(xué)家發(fā)現(xiàn)了引發(fā)帕金森病的隱藏RNA結(jié)構(gòu)
研究人員已經(jīng)確定,G-四聯(lián)體在神經(jīng)退行性疾病中促進(jìn)有害蛋白質(zhì)的聚集。用5-ALA阻斷G4s可以阻止小鼠的帕金森樣癥狀,這為早期疾病干預(yù)提供了一條有希望的途徑。
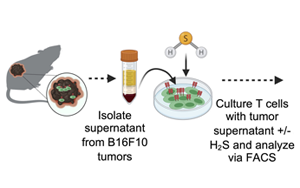
Science Advances:高爾基體越多,T細(xì)胞就越健壯,就越能抗癌!
高爾基體的健康功能與t細(xì)胞殺滅癌細(xì)胞的能力有很大關(guān)系。了解信號(hào)軸如何減輕高爾基應(yīng)激,使其正常工作,為研究人員提供了一個(gè)可能的新的治療靶點(diǎn),以增強(qiáng)t細(xì)胞。不僅如此,Oberholtzer的研究還表明,高爾基體可以作為一種生物標(biāo)志物來(lái)選擇最強(qiáng)的t細(xì)胞進(jìn)行免疫治療。
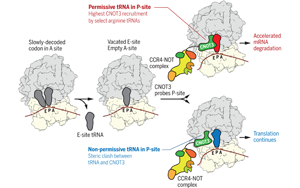
Science:轉(zhuǎn)移RNA調(diào)節(jié)信使RNA的降解
德克薩斯大學(xué)西南醫(yī)學(xué)中心研究人員的一項(xiàng)新研究表明,轉(zhuǎn)移RNA (tRNA)是一種以讀取構(gòu)建蛋白指令而聞名的遺傳分子,在調(diào)節(jié)這些指令在細(xì)胞中持續(xù)的時(shí)間方面也起著關(guān)鍵作用。