摘要:研究針對真核生物中N6-甲基腺嘌呤(6mA)的存在與功能爭議,通過牛津納米孔測序技術對18種單細胞真核生物進行堿基分辨率6mA分析。
在真核生物表觀遺傳學領域,DNA甲基化作為基因表達的關鍵調控機制一直備受關注。5-甲基胞嘧啶(5mC)作為最典型的DNA甲基化形式,其功能和機制已被廣泛研究。然而,另一種甲基化形式——N6-甲基腺嘌呤(6mA)在真核生物中的存在和功能卻長期存在爭議。許多相互矛盾的研究報告使得科學界對6mA在真核基因組中的真實作用莫衷一是。這種不確定性主要源于方法學上的局限性,特別是檢測技術可能帶來的假象。
盡管如此,一些單細胞真系,包括纖毛蟲、早期分支真菌和藻類衣藻,確實顯示出強烈的6mA信號,這引發了關于其起源和進化作用的疑問。為了解決這些爭議,由Alex de Mendoza領導的研究團隊在《Nature Genetics》上發表了突破性研究,通過先進的技術手段揭示了6mA在真核生物中的廣泛存在和進化意義。

圖1 肥胖重塑脂肪組織中CD8+ T細胞的鐵代謝以加劇代謝性炎癥
研究人員應用牛津納米孔測序技術,以堿基對分辨率分析了代表所有主要超群的18種單細胞真核生物的6mA模式。他們發現,強烈的6mA模式僅出現在編碼腺嘌呤甲基轉移酶AMT1的物種中。值得注意的是,6mA持續積累在轉錄起始位點下游,位于H3K4me3標記的核小體之間,表明其與轉錄激活存在保守關聯。
研究團隊采用的主要技術方法包括:對231種真核生物基因組和轉錄組進行MT-A70甲基轉移酶系統發育分析;使用牛津納米孔R9.4.1和R10.4.1技術對18種真核生物進行全基因組DNA測序和修飾堿基識別;通過染色質免疫沉淀測序(ChIP-seq)分析組蛋白修飾H3K4me3和H3K27ac的分布;利用RNA-seq進行基因表達分析;并對四種真核生物進行H3K4me3抑制劑處理實驗,以研究組蛋白修飾與6mA沉積的因果關系。
AMT1是祖先基因但在真核生物中反復丟失
為了闡明MT-A70甲基轉移酶的起源和進化,研究人員檢查了231個真核生物基因組和轉錄組。系統發育分析顯示,MT-A70家族包括六個已確立的真核生物家族:AMT1、AMT6/7、AMT2/5、METTL3、METTL14和METTL4。值得注意的是,原核生物序列形成了一個獨特的進化枝,表明MT-A70具有細菌起源,在真核生物進化早期被繼承。
研究發現,所有六個MT-A70家族都存在于大多數真核生物超群中,表明它們在最后真核生物共同祖先(LECA)之前已經復制。RNA相關的METTL3和METTL14在整個物種系統發育中共同出現,模式類似于DNA相關的AMT1和AMT6/7,表明這兩種酶對在真核生物中具有保守的異源二聚體關聯。
6mA在編碼AMT1的物種中與轉錄相關
基于AMT1的分布,研究人員搜索了具有可檢測基因組6mA的真核生物譜系。為了避免細菌污染,他們專注于無菌培養的物種。研究選擇包括15個編碼AMT1的物種和3個缺乏AMT1直系同源物作為陰性對照的物種。
在所有編碼AMT1的物種中,AT是主要的甲基化背景,盡管AA也顯示出明顯的甲基化水平。ApT位點在所有編碼AMT1的物種中顯示對稱甲基化。相比之下,缺乏AMT1的物種在二核苷酸背景中的差異可忽略不計,AA二核苷酸富集程度最高。
研究人員隨后檢查了6mA的基因組分布。在缺乏AMT1的物種中,6mA在基因和轉座子(TE)中均勻出現,與背景噪聲一致。相反,在編碼AMT1的物種中,AT甲基化峰值出現在轉錄起始位點(TSS)附近。基因內6mA與基因轉錄活性相關。
階段特異性轉錄獨立于6mA發生
研究人員測試了6mA在轉錄變化時的可變性。他們選擇了變形蟲A. castellanii、真菌S. punctatus、魚孢菌C. fragrantissima和C. perkinsii,因為這些生物具有不同的細胞階段,可以在培養中分離。
所有物種在ApT和基因水平分辨率上呈現靜態的6mA甲基化組,大多數基因顯示最小的6mA差異。在N. gruberi中,使用R9納米孔化學稱為甲基化的644個基因,在23°C和30°C下顯示可比較的6mA水平,盡管使用了R10化學和不同的分析流程。當計算階段間差異表達基因的總數,并將這些與沿基因體顯示>1% 6mApT水平變化的基因重疊時,研究人員觀察到數千個基因改變表達而沒有任何可檢測的6mA改變。
5mC和6mA在真核生物中標記不同功能
由于5mC是真核生物中另一種廣泛的DNA甲基化形式,研究人員檢查了其與6mA在他們物種集中的關系。他們發現了多樣的情況——物種表現出不可檢測的5mC水平伴隨高6mA,而其他物種專門含有5mC。一些物種呈現兩種修飾,而盤基網柄菌(Dictyostelium discoideum)兩種都沒有。
研究人員發現,6mA的突變效應在富集區域最為明顯,特別是在TSS后。在大多數物種中,6mA與ApT組成沒有明顯關聯。在一些物種中,甲基化基因比未甲基化基因具有更高的ApT密度,與5mC看到的模式相反。帶有H3K4me3的核小體與6mA共定位
研究結果與先前報告一致,表明6mA在核小體連接DNA中富集。在纖毛蟲中,刪除AMT1破壞了6mA模式,導致TSS周圍核小體定位更加分散。數據集中的大多數物種也顯示周期性6mA模式。
為了探究什么塑造了6mA模式及其與核小體的聯系,研究人員對兩個TSS相關和轉錄活性組蛋白標記——組蛋白3賴氨酸4三甲基化(H3K4me3)和賴氨酸27乙酰化(H3K27ac)進行了染色質免疫沉淀測序(ChIP-seq)。
兩個組蛋白標記顯示預期的TSS后富集,峰值寬度小于1,000 bp。研究人員隨后按H3K4me3信號對基因進行分組,發現6mA與這種組蛋白標記緊密重疊。相比之下,H3K4me3峰值之外的基因組區域在所有物種中具有顯著較低的6mA水平。
為了直接測試H3K4me3沉積是否影響6mA存在,研究人員用H3K4me3抑制劑處理A. castellanii。他們使用OICR-9429和Piribedil,這些抑制劑阻斷WDR5與組蛋白甲基轉移酶的相互作用。兩種抑制劑導致H3K4me3水平的劑量依賴性降低,而總H3水平不受影響。在最高抑制劑濃度下,研究人員分析了處理和DMSO對照樣品中的6mA甲基化組。此外,6mA水平在抑制劑和對照組之間顯示最小差異,無論是全局還是在H3K4me3峰值上,表明H3K4me3不直接決定這些物種中的6mA沉積。
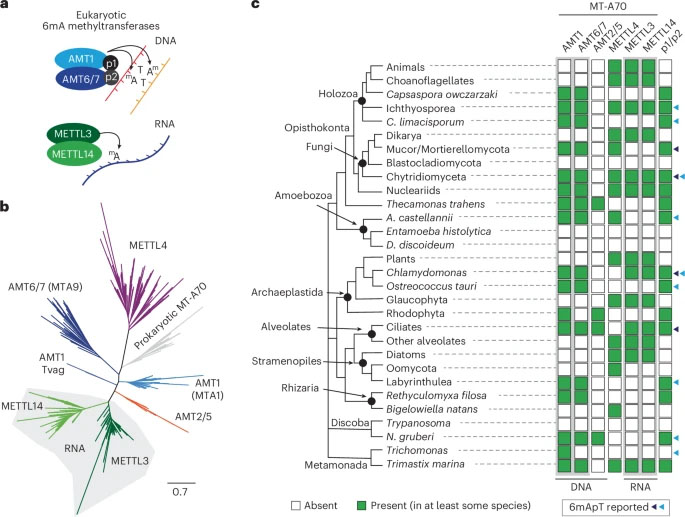
圖2 MT-A70 6-甲基腺嘌呤甲基轉移酶的起源與反復丟失
這項研究證實了6mA在真核生物中的廣泛存在,并追蹤其起源至最后真核生物共同祖先(LECA)。廣泛的采樣支持了一個祖先的AMT1通路,與真核生物生命樹的有爭議的根位置無關。與5mC DNMTs通過獨立細菌轉移被LECA獲取不同,6mA MT-A70甲基轉移酶可能通過單一事件從細菌供體繼承。
研究證實牛津納米孔作為6mA檢測的可靠平臺,展示了在具有不同基因組組成的物種中強大且可重復的模式。長讀長堿基對分辨率圖譜避免了其他方法的缺陷。作為一個例子,在T. vaginalis中,基于抗體的下拉表明6mA在Maverick反轉錄轉座子中富集,其中短讀長映射偽像很常見。相比之下,納米孔數據在轉錄基因上顯示強烈的周期性6mA模式,而在TE中沒有富集,與其他真核生物的模式一致。
AMT1通路反復丟失的發現挑戰了關于DNA甲基化進化的假設。與DNMTs和RNA m6A METTL3/METTL14通路類似,6mA-AMT1通路在真核生物中經常丟失。由于6mA沒有明顯的突變效應,這些丟失可能反映了進化偶然性,6mA的作用被替代機制補償。這在現存真核生物中產生了6mA和5mC的不同組合。
因此,6mA與轉錄強烈相關,在高度表達基因中富集,但其動態性似乎有限。在數據集中的五個物種中,6mA在轉錄擾動下顯示微小變化。在另一個最近發表的例子中,真菌Phycomyces blakesleeanus和Mucor lusitanicus也顯示適度的6mA動態,盡管有處理特定的轉錄變化。類似地,纖毛蟲和M. lusitanicus中的AMT1敲除導致有限的轉錄變化,而發育轉錄變化很少改變5mC模式。
6mA在核小體定位中的功能仍不清楚,因為具有突變AMT1的纖毛蟲表現無序核小體,但通常仍然可行,主要在性繁殖中致命地受影響。考慮到H3K4me3作為TSS后標記的廣泛存在,即使在缺乏6mA的物種中,后者可能非必需或容易在該區域被替代。值得注意的是,H3K4me3和H2A.Z通常與真核生物中的5mC反相關,因此H3K4me3-6mA聯系可能進一步促進染色質區室化。
在魚孢菌中,p1 PHD域表明可能的H3K4me3識別。因此,H3K4me3-6mA之間的層次關系可能獨立進化,或者它們的共存可能僅僅反映轉錄的下游結果,而不是直接因果聯系。生物物理上,6mA被認為降低雙鏈DNA穩定性,這種效應可能有利于高度表達基因起始處的轉錄。然而,要理解6mA作為表觀遺傳標記的作用,識別潛在閱讀器是關鍵。類似地,盡管5mC使DNA變硬,但其在真核生物中的功能更依賴于相關閱讀器或抑制轉錄因子結合,而不是內在生物物理特性。
有趣的是,5mC主要保留在主要多細胞真核生物譜系(植物、動物和雙核菌)中,而AMT1-6mA通路在這些譜系中丟失。在植物和動物中,5mC進化為甲基化基因體,取代TSS后區域中的6mA,但這種替代不可能是6mA丟失的唯一原因。植物和動物的單細胞親屬具有與6mA共存的基因體5mC,表明6mA和5mC具有獨特作用,即使發現在相同區域。
總之,這些數據重塑了對6mA功能和進化的理解,強調6mA和5mC都是原始真核生物染色質工具包的組成部分。盡管纖毛蟲引領了我們對真核生物中6mA的理解,它們 drastically 不尋常的基因組組織,具有小核和大核,以及MT-A70s的譜系特異性擴展,將受益于來自替代譜系的補充見解。通過將分類單元采樣擴展到具有規范基因組的易處理物種,這項工作為闡明6mA功能和理解為什么該通路在主要多細胞譜系中丟失奠定了基礎。
參考資料
[1] Adenine DNA methylation associated with transcriptionally permissive chromatin is widespread across eukaryotes
摘要:研究針對真核生物中N6-甲基腺嘌呤(6mA)的存在與功能爭議,通過牛津納米孔測序技術對18種單細胞真核生物進行堿基分辨率6mA分析。
在真核生物表觀遺傳學領域,DNA甲基化作為基因表達的關鍵調控機制一直備受關注。5-甲基胞嘧啶(5mC)作為最典型的DNA甲基化形式,其功能和機制已被廣泛研究。然而,另一種甲基化形式——N6-甲基腺嘌呤(6mA)在真核生物中的存在和功能卻長期存在爭議。許多相互矛盾的研究報告使得科學界對6mA在真核基因組中的真實作用莫衷一是。這種不確定性主要源于方法學上的局限性,特別是檢測技術可能帶來的假象。
盡管如此,一些單細胞真系,包括纖毛蟲、早期分支真菌和藻類衣藻,確實顯示出強烈的6mA信號,這引發了關于其起源和進化作用的疑問。為了解決這些爭議,由Alex de Mendoza領導的研究團隊在《Nature Genetics》上發表了突破性研究,通過先進的技術手段揭示了6mA在真核生物中的廣泛存在和進化意義。

圖1 肥胖重塑脂肪組織中CD8+ T細胞的鐵代謝以加劇代謝性炎癥
研究人員應用牛津納米孔測序技術,以堿基對分辨率分析了代表所有主要超群的18種單細胞真核生物的6mA模式。他們發現,強烈的6mA模式僅出現在編碼腺嘌呤甲基轉移酶AMT1的物種中。值得注意的是,6mA持續積累在轉錄起始位點下游,位于H3K4me3標記的核小體之間,表明其與轉錄激活存在保守關聯。
研究團隊采用的主要技術方法包括:對231種真核生物基因組和轉錄組進行MT-A70甲基轉移酶系統發育分析;使用牛津納米孔R9.4.1和R10.4.1技術對18種真核生物進行全基因組DNA測序和修飾堿基識別;通過染色質免疫沉淀測序(ChIP-seq)分析組蛋白修飾H3K4me3和H3K27ac的分布;利用RNA-seq進行基因表達分析;并對四種真核生物進行H3K4me3抑制劑處理實驗,以研究組蛋白修飾與6mA沉積的因果關系。
AMT1是祖先基因但在真核生物中反復丟失
為了闡明MT-A70甲基轉移酶的起源和進化,研究人員檢查了231個真核生物基因組和轉錄組。系統發育分析顯示,MT-A70家族包括六個已確立的真核生物家族:AMT1、AMT6/7、AMT2/5、METTL3、METTL14和METTL4。值得注意的是,原核生物序列形成了一個獨特的進化枝,表明MT-A70具有細菌起源,在真核生物進化早期被繼承。
研究發現,所有六個MT-A70家族都存在于大多數真核生物超群中,表明它們在最后真核生物共同祖先(LECA)之前已經復制。RNA相關的METTL3和METTL14在整個物種系統發育中共同出現,模式類似于DNA相關的AMT1和AMT6/7,表明這兩種酶對在真核生物中具有保守的異源二聚體關聯。
6mA在編碼AMT1的物種中與轉錄相關
基于AMT1的分布,研究人員搜索了具有可檢測基因組6mA的真核生物譜系。為了避免細菌污染,他們專注于無菌培養的物種。研究選擇包括15個編碼AMT1的物種和3個缺乏AMT1直系同源物作為陰性對照的物種。
在所有編碼AMT1的物種中,AT是主要的甲基化背景,盡管AA也顯示出明顯的甲基化水平。ApT位點在所有編碼AMT1的物種中顯示對稱甲基化。相比之下,缺乏AMT1的物種在二核苷酸背景中的差異可忽略不計,AA二核苷酸富集程度最高。
研究人員隨后檢查了6mA的基因組分布。在缺乏AMT1的物種中,6mA在基因和轉座子(TE)中均勻出現,與背景噪聲一致。相反,在編碼AMT1的物種中,AT甲基化峰值出現在轉錄起始位點(TSS)附近。基因內6mA與基因轉錄活性相關。
階段特異性轉錄獨立于6mA發生
研究人員測試了6mA在轉錄變化時的可變性。他們選擇了變形蟲A. castellanii、真菌S. punctatus、魚孢菌C. fragrantissima和C. perkinsii,因為這些生物具有不同的細胞階段,可以在培養中分離。
所有物種在ApT和基因水平分辨率上呈現靜態的6mA甲基化組,大多數基因顯示最小的6mA差異。在N. gruberi中,使用R9納米孔化學稱為甲基化的644個基因,在23°C和30°C下顯示可比較的6mA水平,盡管使用了R10化學和不同的分析流程。當計算階段間差異表達基因的總數,并將這些與沿基因體顯示>1% 6mApT水平變化的基因重疊時,研究人員觀察到數千個基因改變表達而沒有任何可檢測的6mA改變。
5mC和6mA在真核生物中標記不同功能
由于5mC是真核生物中另一種廣泛的DNA甲基化形式,研究人員檢查了其與6mA在他們物種集中的關系。他們發現了多樣的情況——物種表現出不可檢測的5mC水平伴隨高6mA,而其他物種專門含有5mC。一些物種呈現兩種修飾,而盤基網柄菌(Dictyostelium discoideum)兩種都沒有。
研究人員發現,6mA的突變效應在富集區域最為明顯,特別是在TSS后。在大多數物種中,6mA與ApT組成沒有明顯關聯。在一些物種中,甲基化基因比未甲基化基因具有更高的ApT密度,與5mC看到的模式相反。帶有H3K4me3的核小體與6mA共定位
研究結果與先前報告一致,表明6mA在核小體連接DNA中富集。在纖毛蟲中,刪除AMT1破壞了6mA模式,導致TSS周圍核小體定位更加分散。數據集中的大多數物種也顯示周期性6mA模式。
為了探究什么塑造了6mA模式及其與核小體的聯系,研究人員對兩個TSS相關和轉錄活性組蛋白標記——組蛋白3賴氨酸4三甲基化(H3K4me3)和賴氨酸27乙酰化(H3K27ac)進行了染色質免疫沉淀測序(ChIP-seq)。
兩個組蛋白標記顯示預期的TSS后富集,峰值寬度小于1,000 bp。研究人員隨后按H3K4me3信號對基因進行分組,發現6mA與這種組蛋白標記緊密重疊。相比之下,H3K4me3峰值之外的基因組區域在所有物種中具有顯著較低的6mA水平。
為了直接測試H3K4me3沉積是否影響6mA存在,研究人員用H3K4me3抑制劑處理A. castellanii。他們使用OICR-9429和Piribedil,這些抑制劑阻斷WDR5與組蛋白甲基轉移酶的相互作用。兩種抑制劑導致H3K4me3水平的劑量依賴性降低,而總H3水平不受影響。在最高抑制劑濃度下,研究人員分析了處理和DMSO對照樣品中的6mA甲基化組。此外,6mA水平在抑制劑和對照組之間顯示最小差異,無論是全局還是在H3K4me3峰值上,表明H3K4me3不直接決定這些物種中的6mA沉積。

圖2 MT-A70 6-甲基腺嘌呤甲基轉移酶的起源與反復丟失
這項研究證實了6mA在真核生物中的廣泛存在,并追蹤其起源至最后真核生物共同祖先(LECA)。廣泛的采樣支持了一個祖先的AMT1通路,與真核生物生命樹的有爭議的根位置無關。與5mC DNMTs通過獨立細菌轉移被LECA獲取不同,6mA MT-A70甲基轉移酶可能通過單一事件從細菌供體繼承。
研究證實牛津納米孔作為6mA檢測的可靠平臺,展示了在具有不同基因組組成的物種中強大且可重復的模式。長讀長堿基對分辨率圖譜避免了其他方法的缺陷。作為一個例子,在T. vaginalis中,基于抗體的下拉表明6mA在Maverick反轉錄轉座子中富集,其中短讀長映射偽像很常見。相比之下,納米孔數據在轉錄基因上顯示強烈的周期性6mA模式,而在TE中沒有富集,與其他真核生物的模式一致。
AMT1通路反復丟失的發現挑戰了關于DNA甲基化進化的假設。與DNMTs和RNA m6A METTL3/METTL14通路類似,6mA-AMT1通路在真核生物中經常丟失。由于6mA沒有明顯的突變效應,這些丟失可能反映了進化偶然性,6mA的作用被替代機制補償。這在現存真核生物中產生了6mA和5mC的不同組合。
因此,6mA與轉錄強烈相關,在高度表達基因中富集,但其動態性似乎有限。在數據集中的五個物種中,6mA在轉錄擾動下顯示微小變化。在另一個最近發表的例子中,真菌Phycomyces blakesleeanus和Mucor lusitanicus也顯示適度的6mA動態,盡管有處理特定的轉錄變化。類似地,纖毛蟲和M. lusitanicus中的AMT1敲除導致有限的轉錄變化,而發育轉錄變化很少改變5mC模式。
6mA在核小體定位中的功能仍不清楚,因為具有突變AMT1的纖毛蟲表現無序核小體,但通常仍然可行,主要在性繁殖中致命地受影響。考慮到H3K4me3作為TSS后標記的廣泛存在,即使在缺乏6mA的物種中,后者可能非必需或容易在該區域被替代。值得注意的是,H3K4me3和H2A.Z通常與真核生物中的5mC反相關,因此H3K4me3-6mA聯系可能進一步促進染色質區室化。
在魚孢菌中,p1 PHD域表明可能的H3K4me3識別。因此,H3K4me3-6mA之間的層次關系可能獨立進化,或者它們的共存可能僅僅反映轉錄的下游結果,而不是直接因果聯系。生物物理上,6mA被認為降低雙鏈DNA穩定性,這種效應可能有利于高度表達基因起始處的轉錄。然而,要理解6mA作為表觀遺傳標記的作用,識別潛在閱讀器是關鍵。類似地,盡管5mC使DNA變硬,但其在真核生物中的功能更依賴于相關閱讀器或抑制轉錄因子結合,而不是內在生物物理特性。
有趣的是,5mC主要保留在主要多細胞真核生物譜系(植物、動物和雙核菌)中,而AMT1-6mA通路在這些譜系中丟失。在植物和動物中,5mC進化為甲基化基因體,取代TSS后區域中的6mA,但這種替代不可能是6mA丟失的唯一原因。植物和動物的單細胞親屬具有與6mA共存的基因體5mC,表明6mA和5mC具有獨特作用,即使發現在相同區域。
總之,這些數據重塑了對6mA功能和進化的理解,強調6mA和5mC都是原始真核生物染色質工具包的組成部分。盡管纖毛蟲引領了我們對真核生物中6mA的理解,它們 drastically 不尋常的基因組組織,具有小核和大核,以及MT-A70s的譜系特異性擴展,將受益于來自替代譜系的補充見解。通過將分類單元采樣擴展到具有規范基因組的易處理物種,這項工作為闡明6mA功能和理解為什么該通路在主要多細胞譜系中丟失奠定了基礎。
參考資料
[1] Adenine DNA methylation associated with transcriptionally permissive chromatin is widespread across eukaryotes



